Swiss Health Web
EMH Schweizerischer Ärzteverlag AG
Farnsburgerstrasse 8
CH-4132 Muttenz
+41 (0)61 467 85 55
support@swisshealthweb.ch
www.swisshealtweb.ch

Publié le 05.05.2020
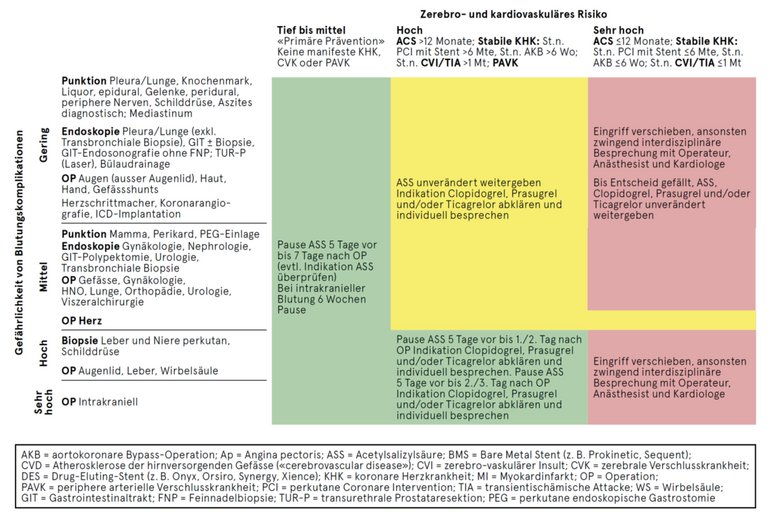
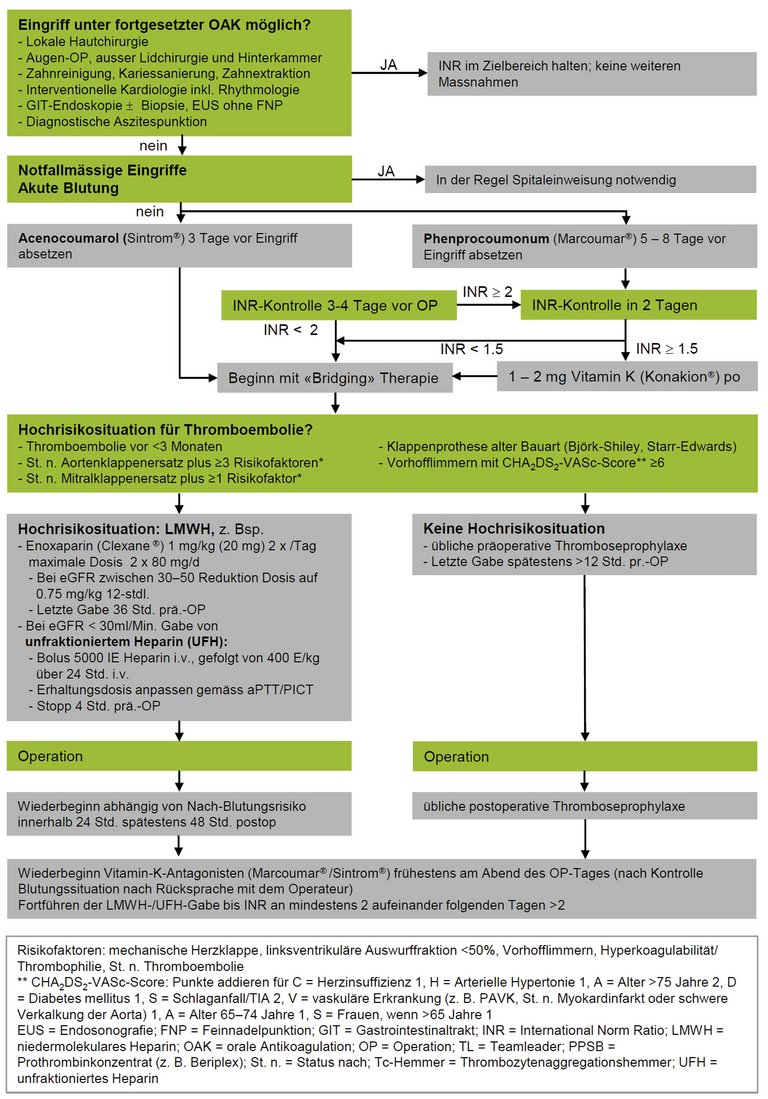
Viele Patientinnen und Patienten, denen ein operativer Eingriff bevorsteht, nehmen gerinnungshemmende Medikamente ein. Täglich stellt sich somit die Frage, ob diese abgesetzt, unverändert weitergeführt oder durch andere Substanzen ersetzt werden sollen.

Publié sous la licence du droit d'auteur.
"Attribution - Non-Commercial - NoDerivatives 4.0"
Pas de réutilisation commerciale sans autorisation..
See: emh.ch/en/emh/rights-and-licences/