Swiss Health Web
EMH Schweizerischer Ärzteverlag AG
Farnsburgerstrasse 8
CH-4132 Muttenz
+41 (0)61 467 85 55
support@swisshealthweb.ch
www.swisshealtweb.ch
Publié le 04.12.2019
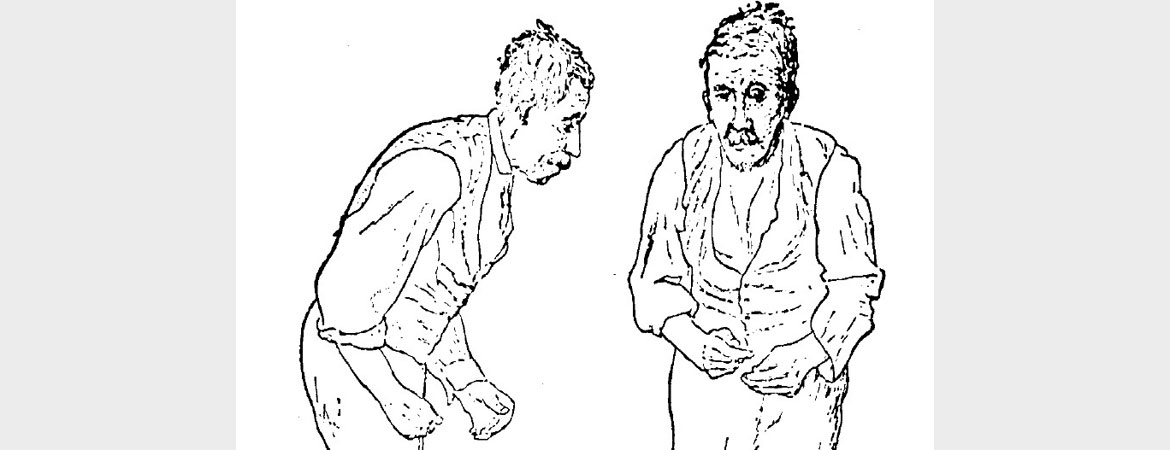
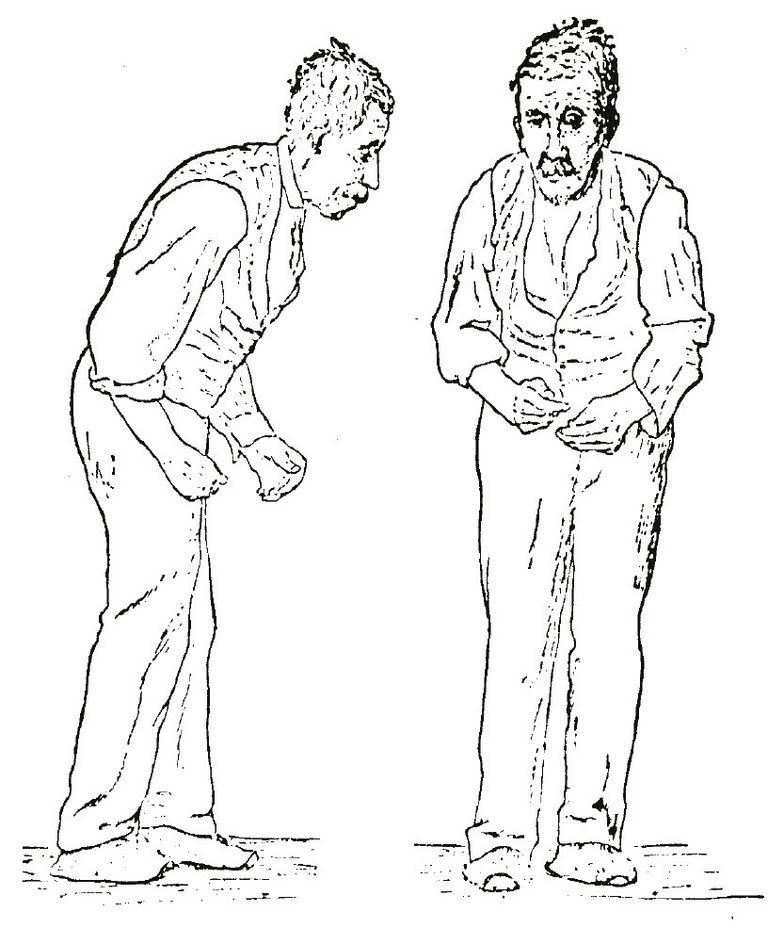
Les patients parkinsoniens doivent plus souvent être hospitalisés en urgence et restent plus longtemps à l’hôpital en raison de complications que les autres patients du même âge. Cet article de revue a été élaboré pour les non-neurologues en vue d’éviter les embûches qui vont de pair avec le diagnostic de la maladie de Parkinson dans le quotidien clinique.

| Tableau 1: Les principaux médicaments antiparkinsoniens en Suisse. | |
| Préparations de lévodopa | |
| •lévodopa/bensérazide: Madopar® • lévodopa/carbidopa: Sinemet®, etc. | Les comprimés de lévodopa sont toujours associés à une substance qui empêche la métabolisation en dehors du SNC. Les préparations sont disponibles dans différents dosages et différentes formes galéniques. La désignation du taux de principe actif diffère selon les fabricants! |
| Agonistes dopaminergiques | |
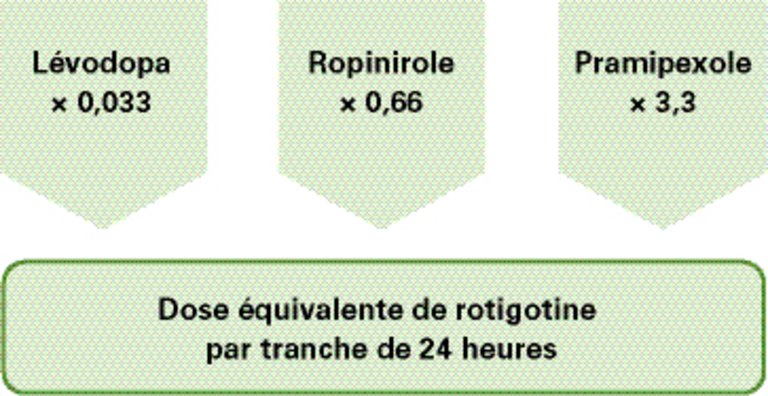
| • ropinirole: Requip®, etc. • pramipexole: Sifrol®, etc. • rotigotine: Neupro® | Les comprimés de ropinirole et pramipexole existent dans des dosages différents sous des formes retard ou non. La rotigotine est administrée par voie transdermique, cf. également le figure 3 dans ce contexte. |
| Inhibiteurs de la COMT | |
| • entacapone: Comtan® • tolcapone: Tasmar® | Les inhibiteurs de la COMT retardent la dégradation de la dopamine et rallongent ainsi indirectement sa demi-vie. Ne peuvent être utilisés qu’avec un traitement par lévodopa! |
| Inhibiteurs de la MAO-B | |
| • rasagiline: Azilect® • safinamide: Xadago® | Les inhibiteurs de la MAO-B retardent la dégradation de la dopamine et rallongent ainsi indirectement sa demi-vie. Xadago® nécessite toujours un traitement concomitant par lévodopa. Tenir compte des interactions avec de nombreux médicaments! |
| Amantadine | |
| • sulfate d’amantadine: PK-Merz® • amantadine hydrochloride: Symmetrel® | Substances rarement utilisées qui agissent via un mécanisme non dopaminergique. Dans certains cas d’urgence, le sulfate d’amantadine (PK-Merz®) i.v. est pratique. Surveiller la fonction rénale et l’intervalle QT! |
| Anticholinergiques | |
| • bipéridène: Akineton® | Agit via un mécanisme d’action non dopaminergique. Profil d’effets indésirables très défavorable! Akineton® i.v. est toutefois pratique dans certains cas d’urgence. |
| Apomorphine | |
| • apomorphine: APO-GO®, Dacepton®, etc. | Il s’agit également d’un agoniste dopaminergique, mais seulement pour une utilisation sous-cutanée, par ex. au moyen d’un stylo injecteur ou d’une pompe à perfusion (comme pour l’administration d’insuline). Nausées en tant qu’effet indésirable (surtout au début du traitement). Ne doit pas être administré avec de l’ondansétron. |
| Tableau 2: Antagonistes des récepteurs dopaminergiques autorisés en cas de Parkinson. |
| • Clozapine: Pour le traitement des symptômes neuropsychiatriques gênants. Toujours procéder selon la devise «start low and go slow». Dose de départ: 6,25 mg. Augmentation lente jusqu’à 100 mg/j en cas de besoin. Hémogramme régulier nécessaire en raison du risque d’agranulocytose! Pas d’association avec le métamizole. |
| • Quétiapine: Même utilisation que la clozapine, mais pas aussi puissante. Appréciée, car pas d’hémogrammes nécessaires. Dose de départ: 12,5 mg. Augmentation lente jusqu’à 100 mg/j en cas de besoin. |
| • Dompéridone: Pour le traitement des nausées, jusqu’à 3x10 mg/j. Les comprimés orodispersibles et la suspension sont pratiques. Il n’existe pas de forme i.v. Attention: Surveiller l’intervalle QT! Tenir compte des médicaments d’association! |
| Tableau 3: Diagnostic de l’état confusionnel aigu au moyen de la Confusion Assessment Method (CAM). |
| 1) Acute Onset and Fluctuating Course: Dégradation aiguë des fonctions cognitives (par rapport à l’état habituel) avec fluctuations au cours de la journée. |
| et |
| 2) Inattention: Diminution de l’attention, c’est-à-dire paraît distrait, a des difficultés à suivre une conversation ou à exécuter une action jusqu’à sa fin. Nous vérifions par ex. la capacité à citer les mois et les jours de la semaine en sens inverse. |
| et |
| 3) Disorganized Thinking: Les déclarations sont-elles cohérentes et adaptées au contexte de la conversation? Passages inattendus d’un thème à l’autre? |
| ou |
| 4) Altered Level of Consciousness: Changement de l’état de veille: hypervigilance, normal, léthargique, somnolent ou soporeux? |
| Un état confusionnel aigu peut être diagnostiqué lorsque les critères 1) et 2) et 3) ou 4) sont remplis. De plus, l’inversion du rythme jour-nuit est typique en cas d’état confusionnel aigu, mais elle ne compte pas parmi les critères formels du Confusion Assessment Method. Rédigé d’après: Inouye et al. Ann Internal Med. 1990;113(12):941–8. |
Publié sous la licence du droit d'auteur.
"Attribution - Non-Commercial - NoDerivatives 4.0"
Pas de réutilisation commerciale sans autorisation..
See: emh.ch/en/emh/rights-and-licences/